肝纤维化是慢性肝病向肝硬化与肝癌发展的必经之路与关键转折点,一旦进入此阶段,疾病将加速迈向不可逆的终末阶段,严重威胁患者生命。在疾病状态下,肝脏的自我修复机制失衡,活化的肝星状细胞(HSC)持续转化为肌成纤维细胞,导致细胞外基质过度沉积,从而驱动纤维化发展。这一过程在代谢相关脂肪性肝炎(MASH)中尤为普遍。当前,MASH治疗药物(如Resmetirom、Semaglutide等)主要着眼于改善代谢与炎症,在直接逆转纤维化方面作用有限。因此,寻找能够直接干预纤维化进展、且可成药的核心治疗靶点,是领域内亟待突破的关键瓶颈。
为实现这一治疗目标,寻找可干预的分子靶点成为研究的关键。3月6日,我院丁楅森团队联合华西第二医院曹中炜研究员,中国医学科学院北京协和医学院王辰院士和北京泰德制药公司等在Cell发表题为《Selective targeting of endothelial and perivascular angiocrine ROCK2 treats liver fibrosis》的研究论文。本研究构建了肝纤维化first-in-class新药研发的完整闭环:从发现血管微环境核心靶点ROCK2,到阐明其通过“血管旁分泌”信号驱动疾病的机制,进而以此为基础研发首创新药TDI01,并最终完成临床验证,为靶向血管的抗纤维化新药研发提供了从理论到临床的坚实基础。

长期以来,肝纤维化的研究主要集中于肝星状细胞的激活,而血管系统在其中的主动调控作用被长期忽视。实际上,血管内皮细胞及其周围的肝星状细胞(HSC)并非被动旁观者,而是通过释放“血管旁分泌”(Angiocrine)信号主动推动纤维化进程的关键参与者。
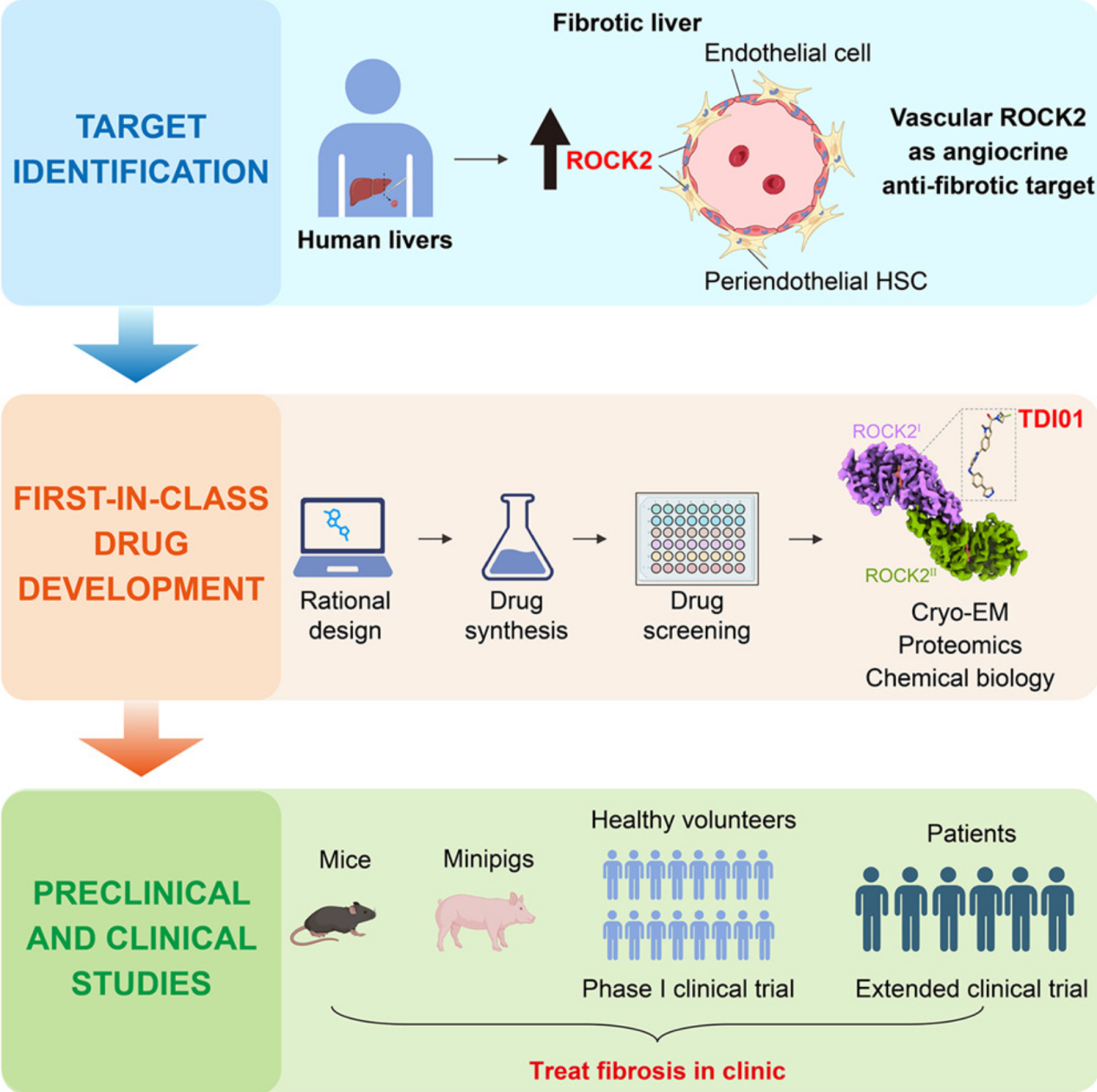
图1 研究路线图
在肝纤维化的研究中,研究团队发现Rho关联卷曲螺旋蛋白激酶-2(ROCK2)在肝内皮细胞和血管周围肝星状细胞特异性上调,而ROCK1的表达无显著变化。机制上,ROCK2的异常激活驱动肝窦内皮窗孔消失和基底膜沉积,即“毛细血管化”(capillarization),其特有的窗孔(fenestration)结构消失,破坏了肝脏血管的物质交换和稳态。同时,ROCK2上调血管旁分泌因子Galectin-3,后者不仅促进炎症与纤维化因子释放,更直接激活肝星状细胞,形成促纤维化循环。逆转肝纤维化的关键在于恢复肝窦血管的Angiocrine功能及生理性“窗孔”表型。因此,靶向血管源ROCK2可同时干预纤维化的结构和功能核心环节。
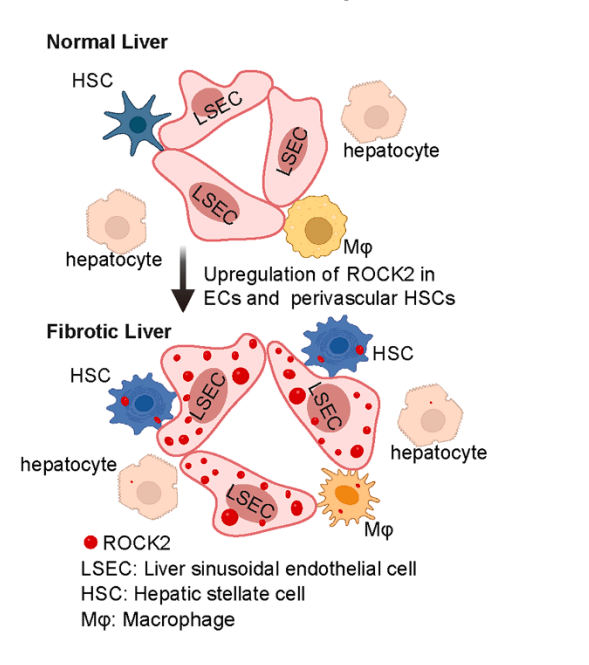
图2 ROCK2在肝血管内皮细胞和血管周肝星状细胞上调
开发高选择性ROCK2抑制剂,精准阻断致病通路同时规避ROCK1带来广谱的副作用,是理想的治疗策略。为实现这一目标,研究团队基于结构进行计算机辅助设计,并结合小鼠与大鼠药代动力学、细胞毒性及心脏毒性等安全性评价,最终优选出先导化合物TDI01。其对ROCK2的IC50为10.31 nM,对ROCK1为6159 nM,选择性比高达598倍。而TDI01能够实现高选择性的核心在于ROCK2与ROCK1在变构口袋边缘的一个关键氨基酸差异。
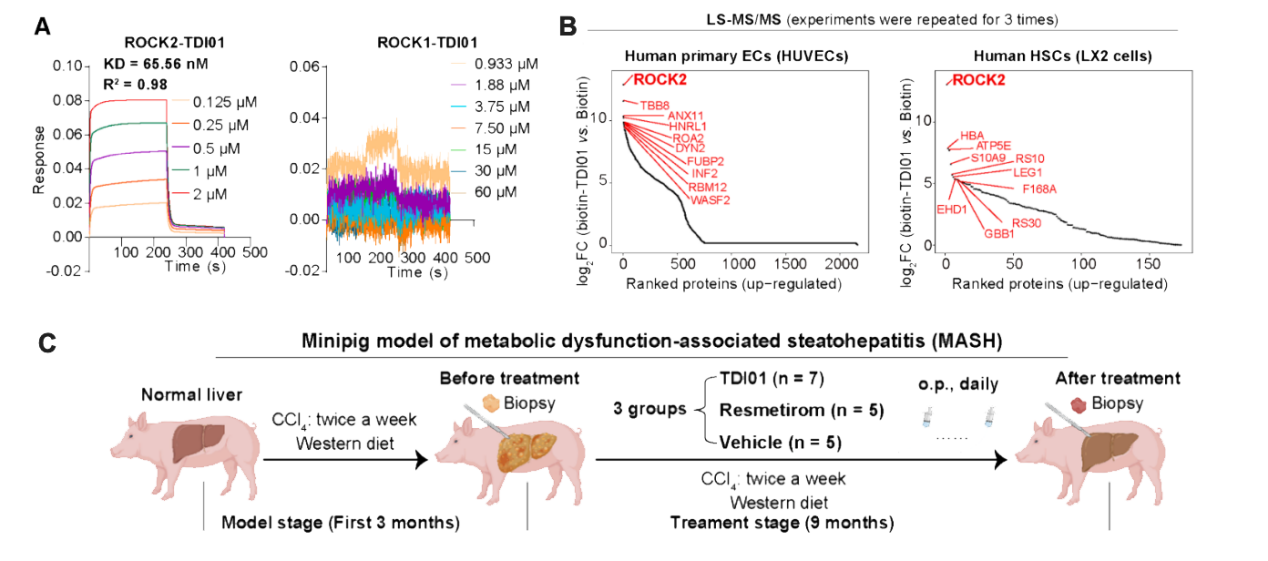
图3 Firs-in-class ROCK2选择性抑制剂在大动物模型中逆转肝纤维化
临床前数据进一步验证了其前景,研究团队不仅利用小鼠纤维化及MASH模型还采用代谢与肝脏结构接近人类的小型猪。在小型猪MASH模型中,TDI01治疗9个月能显著改善纤维化、炎症、脂肪变性并同步改善肝脏硬度与内皮功能。更关键的是,扫描电镜证实TDI01有助于逆转肝窦内皮的病理性“毛细血管化”(capillarization),促进其“开窗”(fenestration)表型的恢复。这一结果验证了TDI01抗纤维化的效果,为临床奠定了基础。
尤为关键的是,团队在临床试验中验证了对于该发现的转化价值,从而形成完整闭环。在人群中,TDI01的1期临床试验首先证实了其在人体内的良好药代动力学特征和安全性。随后,团队在肝纤维化患者中开展了Ib/IIa临床试验。在纳入的6名肝纤维化患者,5名患者在接受TDI01治疗后出现肝纤维化减轻迹象,表现为肝硬度值下降、胶原沉积减少、纤维化分期改善。此外,ROCK2的选择性在人体活检组织中得到直观印证。通过对患者治疗前后肝组织的荧光染色分析发现,TDI01治疗降低了所有6名患者活检样本中磷酸化-ROCK2(pROCK2)的量,而ROCK1和pROCK1的表达则未见明显变化。这一结果直接证实了TDI01在人体内可高选择性地抑制ROCK2,提供了TDI01在真实的人体中靶点特异性抑制的临床证据。
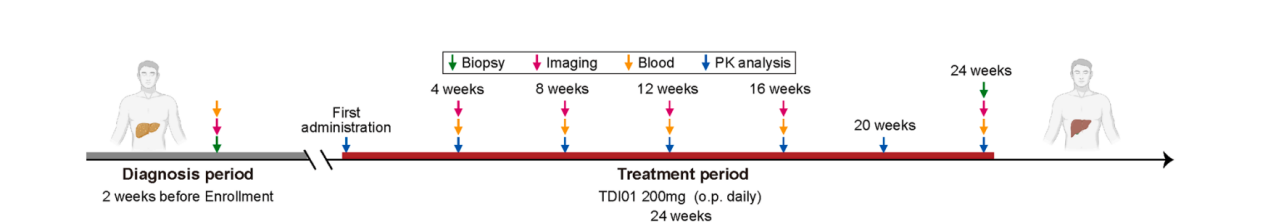
图4 临床试验方案
综上,从Angiocrine机制-药靶-临床验证,靶向血管ROCK2为抗纤维化药物研发提供了一个全链条研究范式。相较于传统抗纤维化策略多抑制胶原合成或促进基质降解,ROCK2选择性抑制剂为肝纤维化治疗领域开辟了新的方向。选择性抑制血管ROCK2从上游阻断纤维化信号通路的传导,修复功能失调的血管微环境Angiocrine功能,阻断驱动纤维化的核心旁分泌信号,从而抑制纤维化的自我维持循环。从Angiocrine机制到临床验证,这项工作不仅证实了靶向血管微环境策略的可行性,更完成了从靶点发现到人体临床试验的first-in-class新药闭环研究。
原文链接:https://www.cell.com/cell/abstract/S0092-8674(26)00166-2